Date: June 2017
Si bien aún se está investigando el aporte directo del CD19 a los cánceres de células B en humanos, su expresión se encuentra en una gran cantidad de neoplasias de células B. Por ejemplo, la leucemia linfoblástica aguda (LLA), los linfomas de células B y las leucemias de células B demuestran una expresión de CD19 del 80%, 88% y 100% respectivamente.1 La LLA se presenta con una producción excesiva de linfoblastos en la médula ósea que se multiplican constantemente hasta generar la inhibición de la producción normal de células hematopoyéticas.
La LLA se encuentra más comúnmente en niños pequeños pero también aparece en adultos más grandes. Los niños presentan una tasa de curación del >80%, mientras que en los adultos la enfermedad tiene una tasa de curación de entre el 20 y el 30%. Una enfermedad similar es la leucemia linfocítica crónica (LLC) que generalmente se diagnostica en adultos más grandes. Tanto la LLA como la LLC se identificaron como neoplasias adecuadas para las terapias dirigidas por CD19. Mientras se investigan los anticuerpos monoclonales anti-CD19 y otros enfoques apropiados para el desarrollo clínico, por amplio margen el enfoque más común para actuar sobre las neoplasias relacionadas con el CD19 son las células T modificadas con receptores de antígenos quiméricos (CAR-T). El CD19 fue la primera diana que se usó para esta estrategia terapéutica con células T y sigue siendo un área de investigación clínica activa.
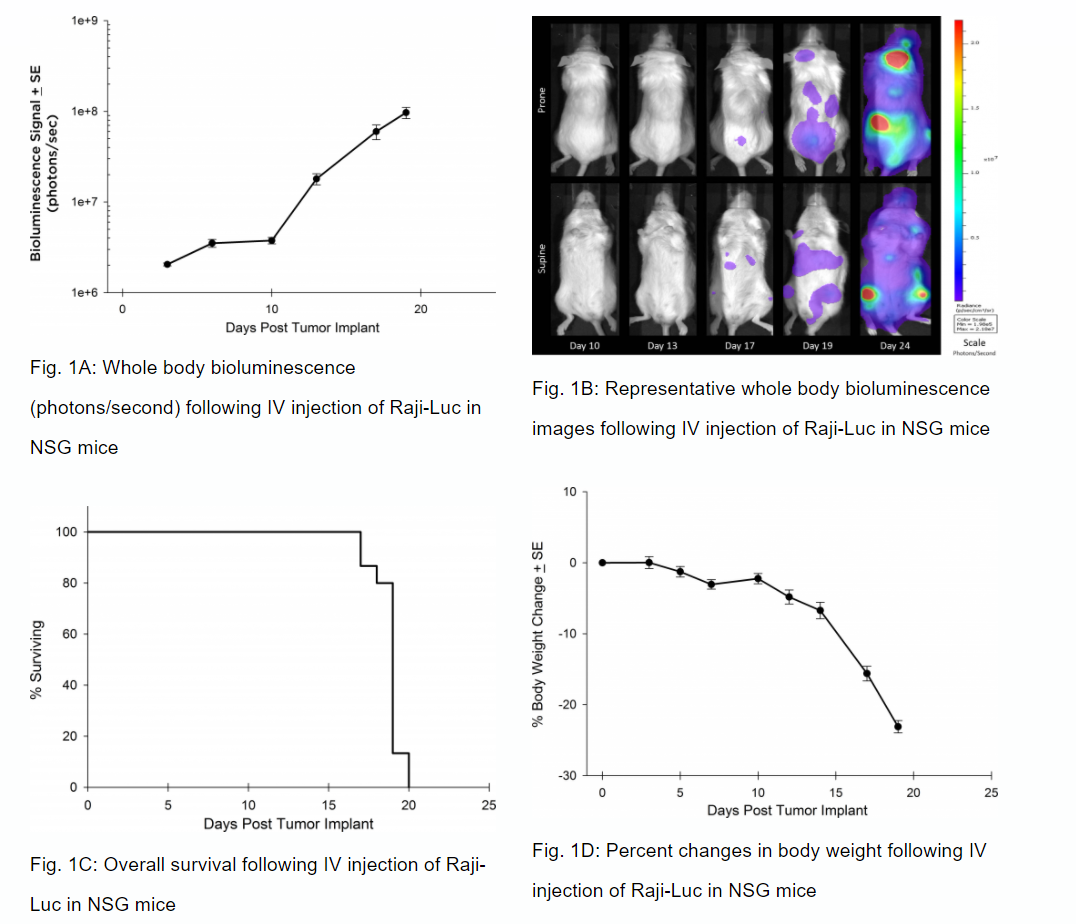
Desde el punto de vista preclínico, la línea celular Raji del linfoma de Burkitt en humanos ha sido un elemento fundamental para determinar la actividad antitumoral para enfoques relacionados con las neoplasias de células B. At Labcorp, we employ a luciferase-expressing Raji cell line (Raji-Luc) to allow us to track disease progression and therapeutic response over time through in vivo optical imaging. Raji-Luc es un modelo excelente para evaluar las terapias con CAR-T dirigidas por CD19. Hemos utilizado este modelo en ratones SCID y NSG para más de una docena de estudios de terapias con células CAR-T u otras terapias celulares. En muchos casos, se requiere la variedad de ratón más inmunodeficiente, NSG, para la supervivencia y persistencia de la terapia celular. De esta manera, validamos el crecimiento de Raji-Luc en ratones NSG mediante imagenología por bioluminiscencia (BLI) in vivo (figuras 1A y B) y hallamos una propagación de la enfermedad que se ilustra mediante un criterio de valoración de sobrevida total de aproximadamente 20 días (morbilidad/mortalidad, figura 1C). De acuerdo con la rápida inducción de la enfermedad, los ratones presentaron una pérdida de peso progresiva (figura 1D) y finalmente una parálisis de las extremidades posteriores que requirió la eutanasia.
Validación del crecimiento de Raji-Luc en ratones NSG
Actividad antitumoral del anticuerpo monoclonal anti-CD20, rituximab
Al igual que el CD19, el CD20 también es un marcador de células B e inicialmente fue una diana de los fármacos utilizados para atacar neoplasias de células B como el linfoma no Hodgkin. El desarrollo clínico del anticuerpo monoclonal anti-CD20, rituximab, fue revolucionario para el uso de anticuerpos monoclonales como terapias oncológicas. En ratones SCID, analizamos la actividad antitumoral de rituximab y comprobamos una sobrevida total mayor (figura 2A) correlacionada con una carga tumoral de cuerpo entero reducida determinada por BLI in vivo (figuras 2B y 2C). Al igual que en los estudios en ratones NSG, observamos signos clínicos de evolución de la enfermedad como parálisis de las extremidades posteriores y pérdida de peso corporal (figura 2D). Además de usar BLI in vivo, también analizamos la incidencia de la enfermedad en varios tejidos mediante BLI ex vivo (tabla 1). Mediante análisis ex vivo, reforzamos la comprobación de que el tratamiento con rituximab redujo la carga total de la enfermedad.
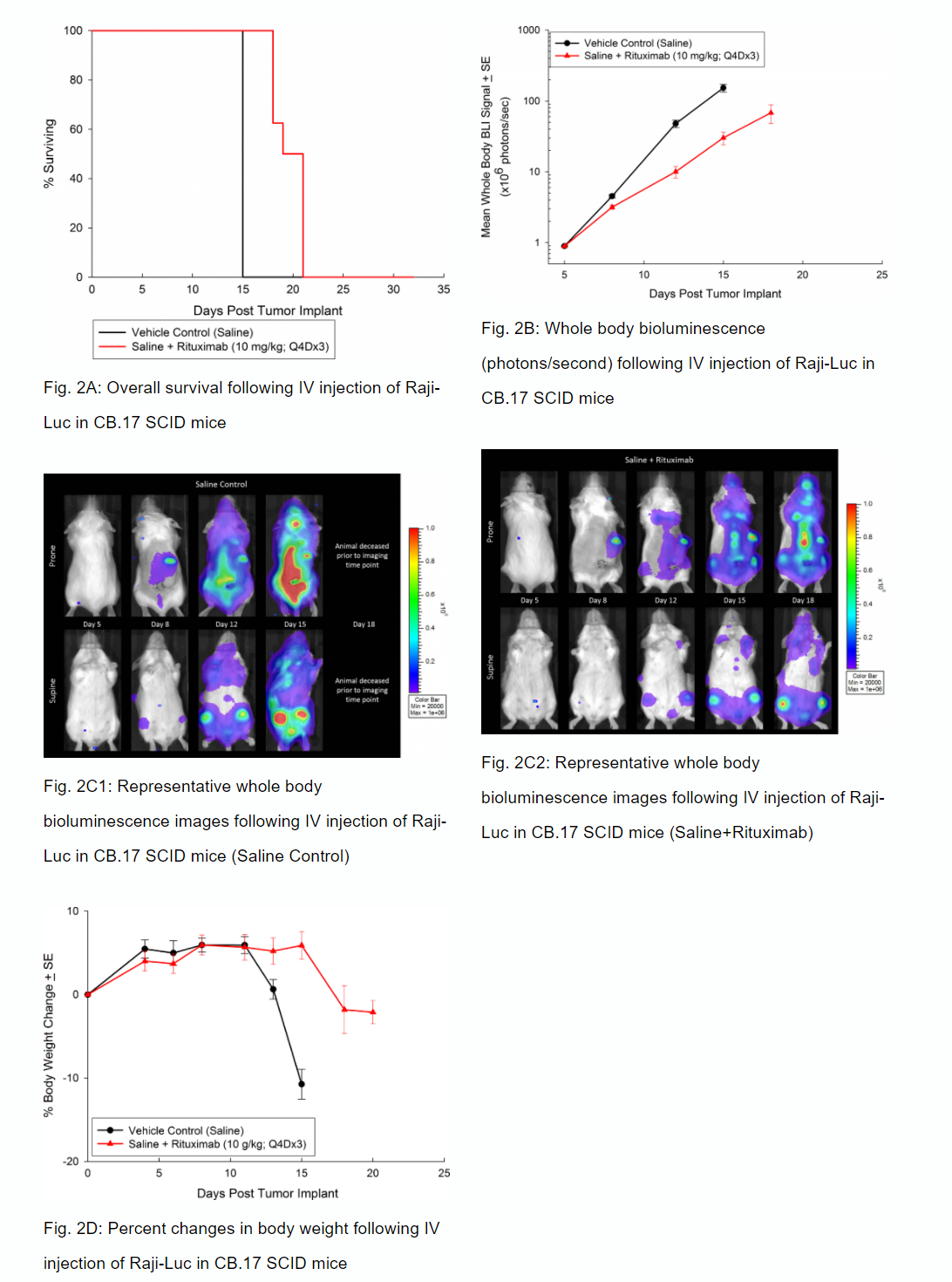
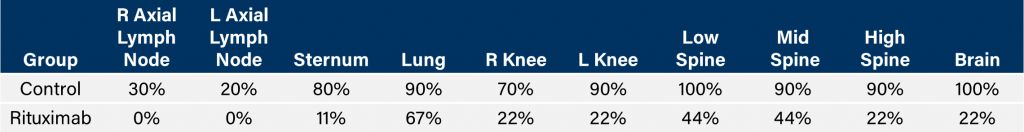
Tabla 1: incidencia de propagación de la enfermedad tras la inyección IV de Raji-Luc en ratones SCID CB.17.
Evaluación del modelo Raji-Luc por vía SC en ratones SCID
Si bien la mayoría de los enfoques terapéuticos utilizaron el modelo Raji-Luc tras la inyección IV, hubo casos en los que las estrategias antitumorales requirieron la evaluación subcutánea (SC). Con este propósito, validamos el crecimiento de la línea Raji-Luc por vía SC en ratones SCID. La línea crece bastante rápido con un tiempo de duplicación de cuatro días y transcurren aproximadamente 27 días desde el implante hasta alcanzar los criterios de eutanasia (figura 3).
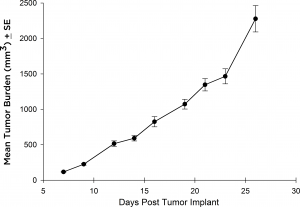
Fig. 3: crecimiento subcutáneo de células Raji-Luc implantadas por vía SC en ratones SCID CB.17
De esta manera, el modelo Raji-Luc en ratones SCID o NSG ofrece un método rápido para el análisis de terapias dirigidas por CD19 o CD20.
Contact us to speak with one of our scientists about how Raji-Luc or one of our other models can be used for your next CAR-T study.
Referencias
Conéctese
Conversemos
Contáctenos