Date: November 2018
Los linfomas son un conjunto de tipos de cáncer de células linfoides que pueden ser de una gravedad variada, desde poco activos a agresivos. Los linfomas derivados de células B, específicamente el linfoma no Hodgkin (LNH), son los más prevalentes, pero esta enfermedad también puede originarse a partir de células T. Se estima que en el 2018 se diagnosticarán 74.680 nuevos casos de LNH en los Estados Unidos y 19.910 pacientes fallecerán a causa de esta enfermedad. Si bien la tasa de supervivencia de cinco años para LNH es relativamente alta en un 71%,[1] la recurrencia es algo común, por lo que es importante seguir buscando tratamientos mejorados para linfoma y mejorar la supervivencia a largo plazo de estos pacientes.
Los investigadores usan modelos preclínicos de linfoma en ratones para explorar nuevas estrategias de combinación de quimioterapia o radiación convencional con agentes inmunomodeladores. To support these efforts, Labcorp has developed the murine B cell lymphoma model, A20. El modelo A20 proviene de un sarcoma de células reticulares espontáneo de un ratón Balb/c anciano.[2] Se ha reportado que los tumores A20 expresan PD-L1,[3], consistente con nuestro perfil de secuenciación de ARN (datos no mostrados) y concordante con varios subtipos de linfoma humano[4], por lo que resulta un modelo atractivo para usar en desarrollo farmacológico de inmunoterapia.
En un artículo destacado sobre modelo de 2017 presentamos los datos de crecimiento iniciales y la respuesta a la terapia iniciada poco después de un implante subcutáneo. En 2018 seguimos trabajando para ampliar la caracterización de este modelo. Aquí presentamos los datos iniciales de respuesta antitumoral en tumores A20 subcutáneos establecidos y la cinética de crecimiento presente de un modelo A20 sistémico activado por luciferasa donde la evolución del tumor se monitoreó mediante imagenología por bioluminiscencia (BLI).
El tratamiento del modelo A20 con agentes de inmunoterapia in vivo es muy eficaz contra la enfermedad en su estadio inicial, con varias respuestas completas. Sin embargo, como era de esperarse, al iniciar el tratamiento una vez que los tumores están establecidos se obtiene una respuesta mucho más limitada. La imagen 1 ilustra el crecimiento individual (A-F) de tumores de control y de aquellos tratados con anti-mPD-1 o anti-mPD-L1 como monoterapia o en combinación con radiación focalizada administrada con SARRP (XStrahl). La terapia combinada produjo una respuesta antitumoral más que acumulativa, lo que indica que estas estrategias se pueden evaluar muy bien en el modelo A20 una vez que los tumores están establecidos. Además, la eficacia de anti-mGITR y anti-mCD137 contra tumores A20 establecidos fue mínima a moderada, lo que daría lugar a un amplio rango dinámico para evaluar mejorías al combinar estos anticuerpos con otros agentes que se estén investigando (imagen 2 A-C).
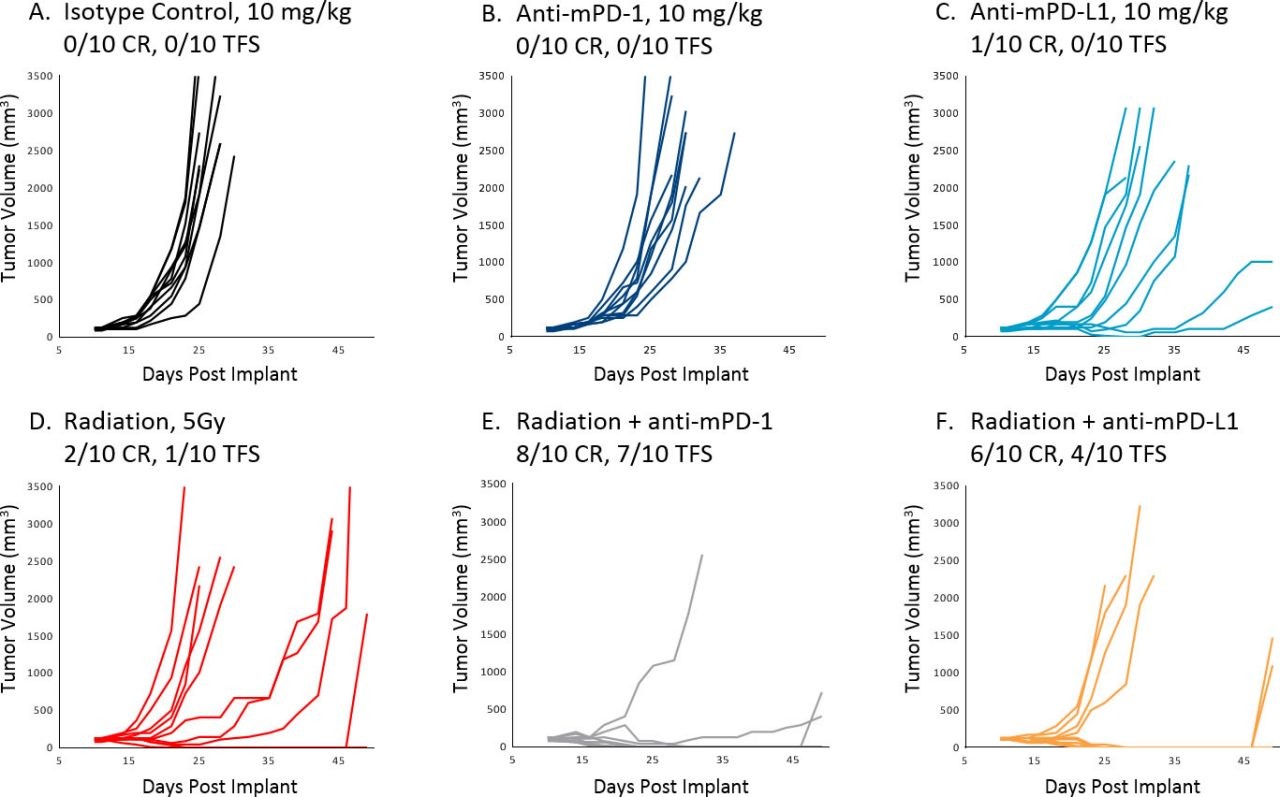
Imagen 1: Respuesta de tumores A20 establecidos a tratamiento; CR = respuesta completa, TFS = sobreviviente sin tumor
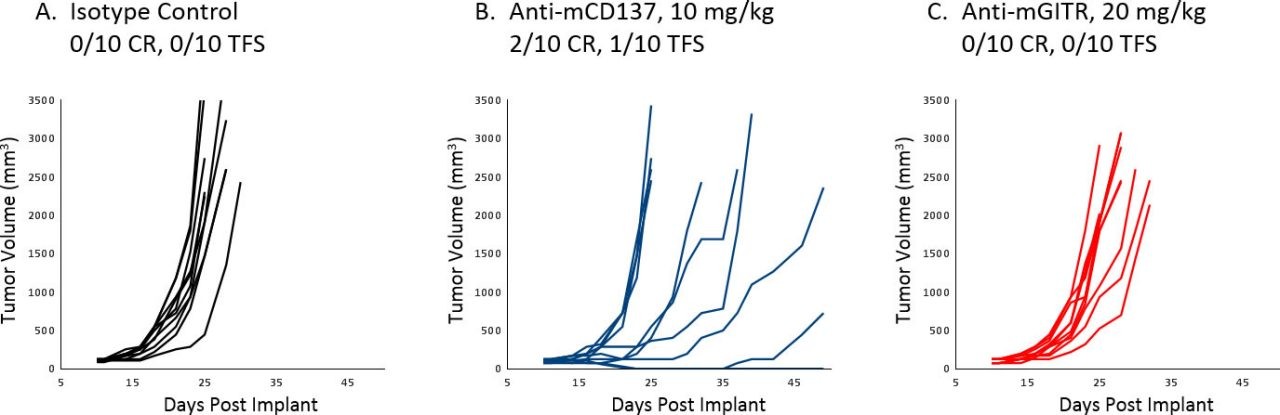
Para aumentar más la utilidad del modelo de linfoma A20, aplicamos luciferasa a la línea celular A20 para que se pueda usar para monitorear la evolución del tumor en un cáncer sistémico. El tiempo de duplicación promedio del modelo es de 2,7 días con una ventana terapéutica de aproximadamente tres semanas.
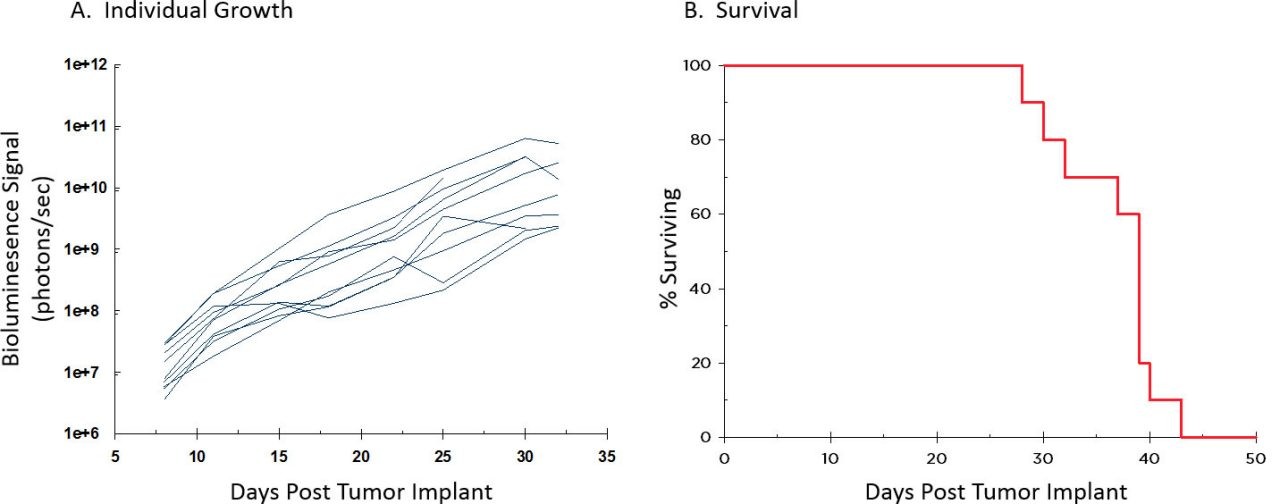
Figura 3: cinética de crecimiento de A20-Luc individual y supervivencia
La figura 3 muestra la evolución de tumores individuales definidos por BLI (A) y supervivencia en general (B) que indica una cinética de crecimiento favorable, y la imagen 4 ilustra imágenes de BLI representativas con el tiempo. Al momento de la necropsia, se registró una incidencia del 100% de lesiones hepáticas y una incidencia del 70% en parálisis de cuarto trasero y/o lesiones en otros órganos (bazo, ovario, páncreas). La distensión abdominal fue un signo clínico común que se manifestó entre los días 30 y 32 y se correlaciona bien con los momentos de una fuerte señal de BLI en las imágenes 3 y 4. Se está haciendo un estudio de seguimiento para investigar la respuesta a bloqueo de puntos de control y moléculas coestimulantes usando este modelo.
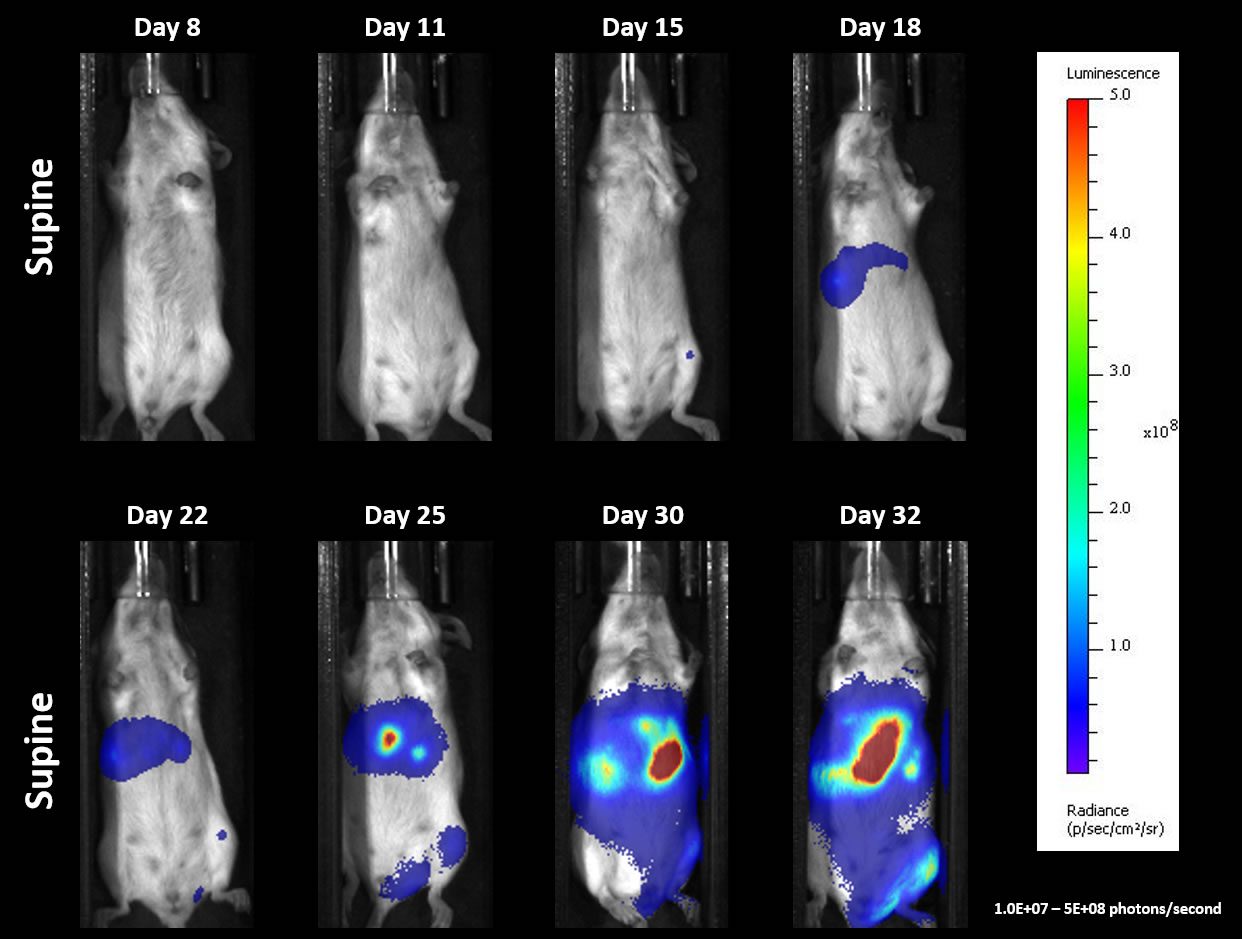
Figura 4: A20-Luc sistémico - Imágenes de BLI representativas con el tiempo
El modelo A20 constituye un sólido medio preclínico para el estudio de linfoma de células B tanto con métodos subcutáneos como sistémicos.
Please contact Labcorp to speak with our scientists about how A20 or one of our other syngeneic models can be used for your next immuno-oncology study.
Referencias
[2] Kim KJ, Kanellopoulos Langevin C, Merwin RM, Sachs DH, Asofsky R (1979) "Establishment and characterization of BALB/c lymphoma lines with B cell properties". Journal of Immunology, 122(2): 549-554.
[3] Sagiv-Barfi I, Kohrt HEK, Czerwinski DK, Ng PP, Chang BY, Levy L (2015) "Therapeutic antitumor immunity by checkpoint blockade is enhanced by ibrutinib, an inhibitor of both BTK and ITK". PNAS, 112(9): E966-E972.
Conéctese
Conversemos
Contáctenos