Autor: Erin Trachet | Directora, Desarrollo Científico
Date: September 2019
El cáncer de mama sigue siendo una de las enfermedades más prolíficas y de riesgo entre mujeres de todo el mundo. Según cifras de la American Cancer Society, entre mujeres estadounidenses en el 2017 hubo aproximadamente 253.000 nuevos casos de cáncer de mama invasivo con 41.000 fallecimientos.[1] Aproximadamente el 6 al 10% de los nuevos casos de cáncer (15.000 a 25,000) se diagnostican como metastásicos (estadio IV). No obstante, se cree que el 20 al 30% de todos los casos de cáncer de mama harán metástasis con el tiempo.[1]
Los modelos animales pueden ser herramientas muy poderosas para analizar el desarrollo y evolución del cáncer. Un ejemplo es el modelo de oncoproteína T media de polioma transgénico (PyMT). La expresión de PyMT está restringido a las glándulas mamarias por el promotor MMTV y da resultado en ratones que atraviesan cuatro estadios diferentes de progresión tumoral desde premaligno a maligno. Estos estadios son comparables al cáncer de mama humano. Además de las similitudes morfológicas con el cáncer de mama humano, la expresión de biomarcadores en tumores inducidos por MMTV-PyMT también concuerda con la asociada a un resultado poco favorable en humanos. Esta expresión incluye la pérdida de receptores de estrógeno y progesterona y la expresión persistente de ErbB2/Neu (Her2) y cyclinD1 en tumores MMTV-PyMT a medida que avanzan hacia el estadio maligno.[2]
Given the desperate need, and the uniqueness of the MMTV-PyMT model, Labcorp has developed and optimized a transplantable version of this model that’s derived from transgenic host mice (FVB/N-Tg(MMTV-PyVT)634Mul/J).
Crecimiento tumoral en el panículo adiposo mamario primario
La cinética de crecimiento del tumor primario ortotópico para el modelo MMTV-PyMT (PyMT) trasplantable se muestra en la imagen 1. El tiempo de duplicación promedio es de ~8 días con un aumento constnte en el volumen tumoral y sin aparente pérdida de peso corporal relacionada con el tumor. Cuando se les practicó la eutanasia a los animales por el crecimiento del tumor primario se detectaron nódulos en los pulmones. La tasa de crecimiento habilita una ventana terapéutica de cuatro semanas para evaluar las respuestas antitumorales.
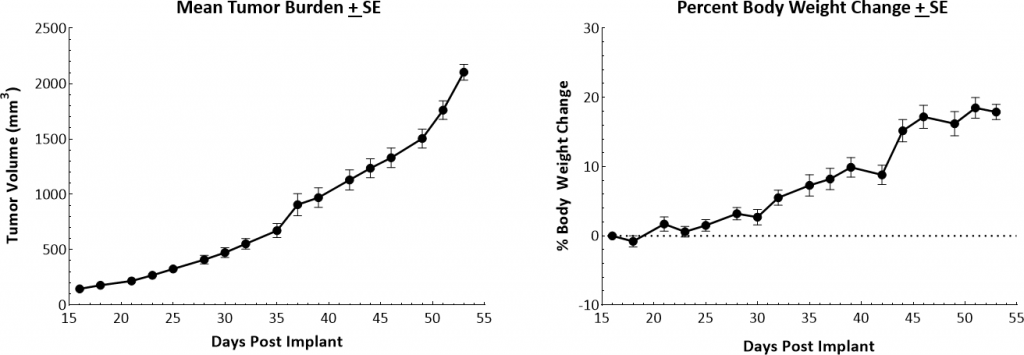
Figura 1: cinética de crecimiento y cambio en el peso corporal de tumores MMTV-PyMT en ratones FVB/NJ hembra.
Perfil inmune de tumores PyMT
The baseline tumor immune composition was analyzed by flow cytometry and is shown in Figure 2. The lymphoid population has an equal distribution of CD8+ and CD4+ T cells. Mientras que las células NK tienen una presencia considerable, las células B y células NKT están mínimamente representadas. Los tumores tienen una gran población mieloide representada predominantemente por CSDM-G y MAT M1. La infiltración de células T CD8+ y células NK respalda la teoría de que el modelo PyMT podría responder a agentes inmunomoduladores. Sin embargo, también se observa una cantidad considerable de células supresoras mieloides dentro del microambiente tumoral. Por ello probamos la respuesta a agentes inmunomoduladores (ver imagen 3) para determinar si el modelo PyMT está más en línea con un tumor "frío" inmunosupresor o un tumor "caliente" inmunosensible.
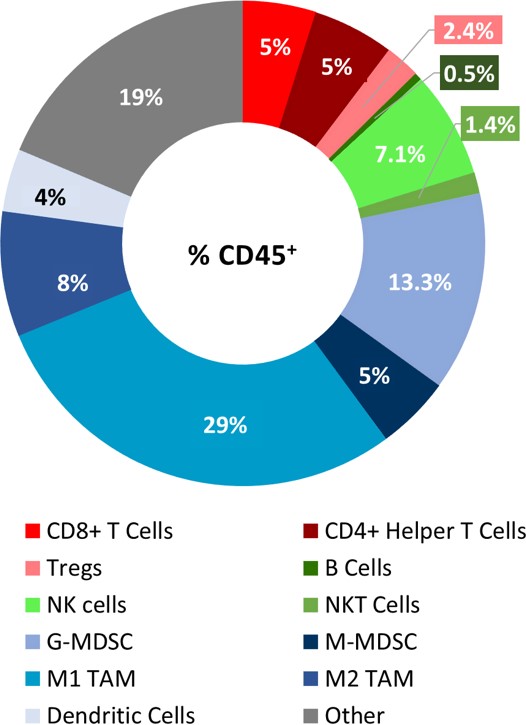
Figura 2: perfil inmune de infiltrados en el tumor PyMT
Respuesta a tratamientos de bloqueo de puntos de control y radiación focalizada
Para evaluar la respuesta antitumoral a agentes inmunomoduladores, se trató a ratones con tumores PyMT ortotópicos con anticuerpos de bloqueo de puntos de control (anti-mPD-1, anti-mPD-L1 y anti-mCTLA-4) y radiación focalizada. Con el tratamiento con inhibidores de puntos de control con un solo agente se observó una respuesta leve con retrasos en el crecimiento tumoral de entre 3 a 6 días pero sin regresión tumoral (imagen 3). Los tumores PyMT ortotópicos son solo marginalmente sensibles al tratamiento con inhibidores de puntos de control, lo que deja una clara oportunidad para que una terapia combinada tenga un mayor beneficio. Además, estos datos sugieren que el modelo entra más dentro de un perfil de tumor "frío".
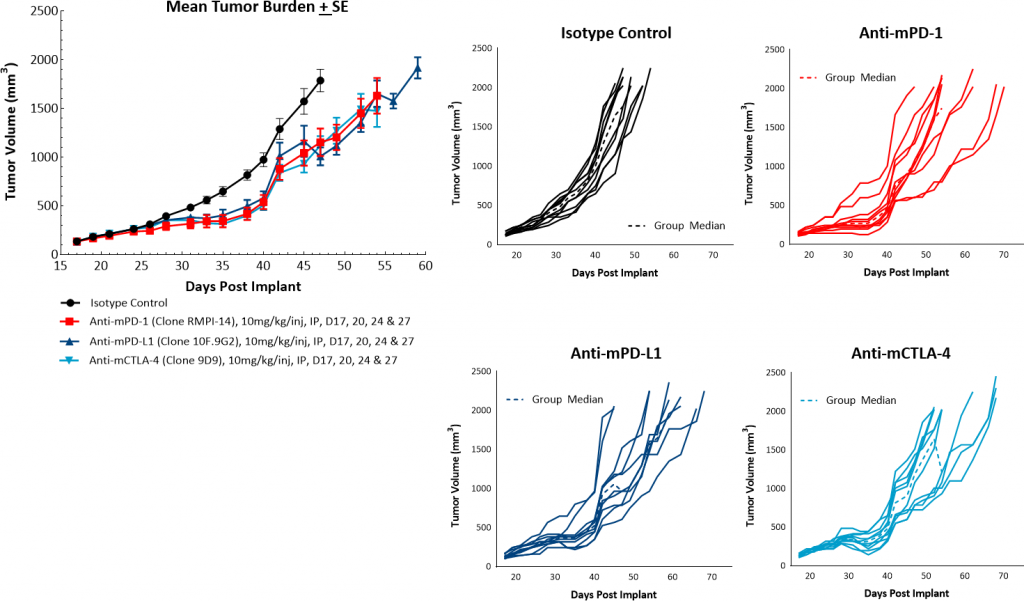
Imagen 3: Respuesta del modelo PyMT a inhibidores de puntos de control.
Además del bloqueo de puntos de control, también se cree que la radiación focalizada es un método de tratamiento útil para modificar un microambiente tumoral inmunosupresor. Asimismo, el tratamiento con radiación es una terapia común para muchos pacientes con cáncer de mama. Labcorp utilizes the Small Animal Radiation Research Platform (SARRP; Xstrahl) to provide focal radiation therapy to mice in a manner consistent with radiation treatment in patients. En este modelo probados una dosis de radiación focalizada de 5, 10 o 20Gy y resultaron bien toleradas y altamente eficaces. Los niveles de dosis de 20 y 10 Gy produjeron una fuerte respuesta antitumoral con una incidencia del 100% y el 38% de respuesta completa respectivamente (imagen 4). Basado en estos datos, para estudios de combinación se recomendaría una sola dosis de radiación focalizada de 5 Gy.
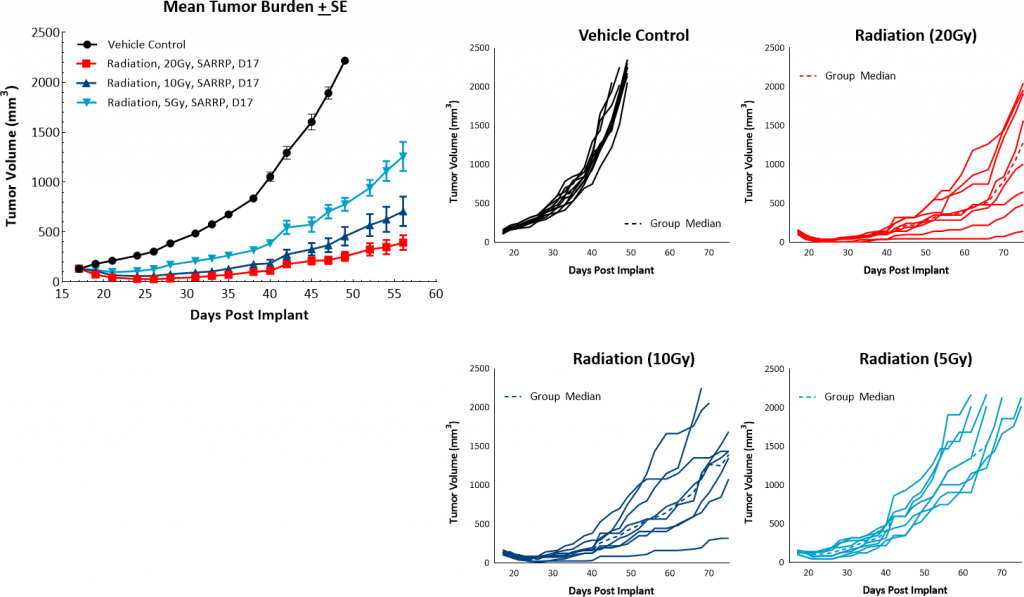
Figura 4: respuesta del modelo PyMT a radiación focalizada.
Panorama
El modelo PyMT trasplantable es un modelo muy útil para evaluar fármacos contra carcinoma de mama. Este modelo ofrece a la comunidad de investigación la capacidad de usar un modelo que imita muchos aspectos y complejidades de la enfermedad clínica. Muchos enfoques clínicos en cáncer de mama ahora están incorporando inmunoterapias y/o radioterapia como parte de ensayos clínicos en curso. Los datos que presentamos sugieren que el modelo PyMT es adecuado para estudios de combinación con inhibidores de puntos de control o radiación focalizada de baja dosis. Contact Labcorp to learn more about our transplantable PyMT model or other breast cancer models that we offer.
Referencias
Conéctese
Conversemos
Contáctenos