Autor: Erin Trachet, Asesora Científica Sénior, Oncología / Gerente Sénior, Desarrollo de Propuestas
Date: September 2017
Más del 90% de todos los cánceres pancreáticos se clasifican como adenocarcinomas ductales y, en occidente, el cáncer pancreático es la cuarta causa principal de muertes relacionadas con cáncer.
El pronóstico con un cáncer pancreático es muy desfavorable, con una tasa de supervivencia relativa de 5 años del 5% y una supervivencia promedio de 3,5 meses para pacientes con tumores irresecables de estadio III.1 Lamentablemente, la incidencia de cáncer pancreático se ha elevado mientras que la tasa de supervivencia de 5 años no ha cambiado. La resección quirúrgica es la única terapia potencialmente curativa, pero solo el 10% son diagnosticados con tiempo suficiente para que esta sea una opción y la mayoría que son elegibles para una cirugía terminan teniendo una recaída. Al igual que con muchos otros tipos de cáncer, el cáncer pancreático crece sigilosamente por años sin ningún tipo de síntoma. En la mayoría de los casos, el diagnóstico recién se hace después de que el cáncer se extendió fuera del páncreas a otros tejidos proximales y/o hizo metástasis. A estos pacientes les quedan muy pocas opciones significativas. Por eso necesitamos con urgencia nuevas terapias para el cáncer pancreático.
Durante los últimos 15 años, a los pacientes diagnosticados con cáncer pancreático avanzado se les ha recetado gemcitabina (Gemzar®) como tratamiento de primera línea estándar. Preclínicamente, usamos gemcitabina como nuestro estándar de atención para dar un parámetro de comparación a nuestros clientes que buscan superar las opciones de tratamiento clínico actuales o combinarlas con terapias nuevas, como agentes focalizados e inmunomoduladores.
Hay varias líneas celulares pancreáticas humanas y murinas a disposición de la comunidad de investigación oncológica preclínica para ayudar en el desarrollo de nuevas terapias. Labcorp cuenta con un gran panel de líneas pancreáticas listas para usar en pruebas (ver cuadro 1). Hemos caracterizado y optimizado el crecimiento subcutáneo (SC) para varios de estos modelos y evaluamos su respuesta a un tratamiento con gemcitabina.
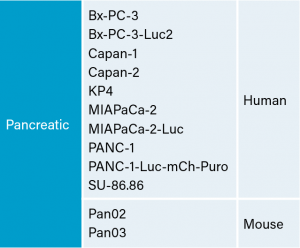
Tabla 1: líneas celulares de carcinoma pancreático en Labcorp
PANC-1
El PANC-1 se aisló de un hombre caucásico de 56 años de edad con adenocarcinoma ductal pancreático. El crecimiento del tumor subcutáneo es consistente y fiable, y el volumen del tumor se duplica cada 5 días y normalmente llega al tamaño de evaluación (~750 mm3) en aproximadamente 29 días después del implante. El tratamiento con gemcitabina (160 mg/kg) se tolera bien y produce un retraso del crecimiento tumoral estadísticamente significativo, pero no es curativo (ver imágenes 1 y 2).
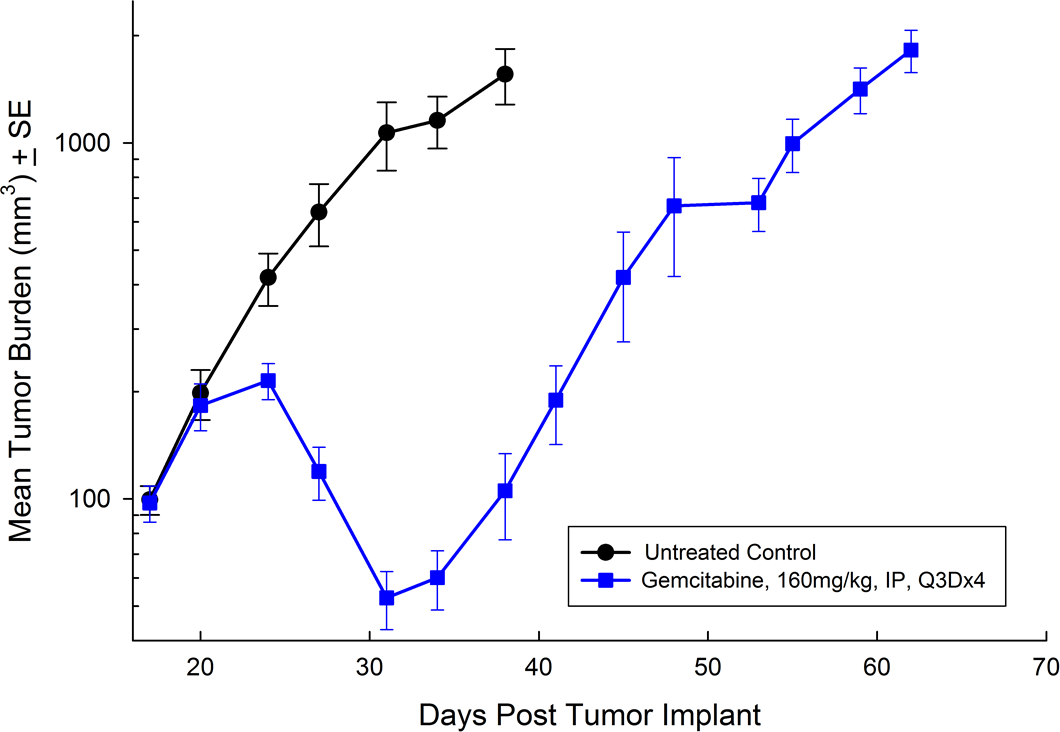
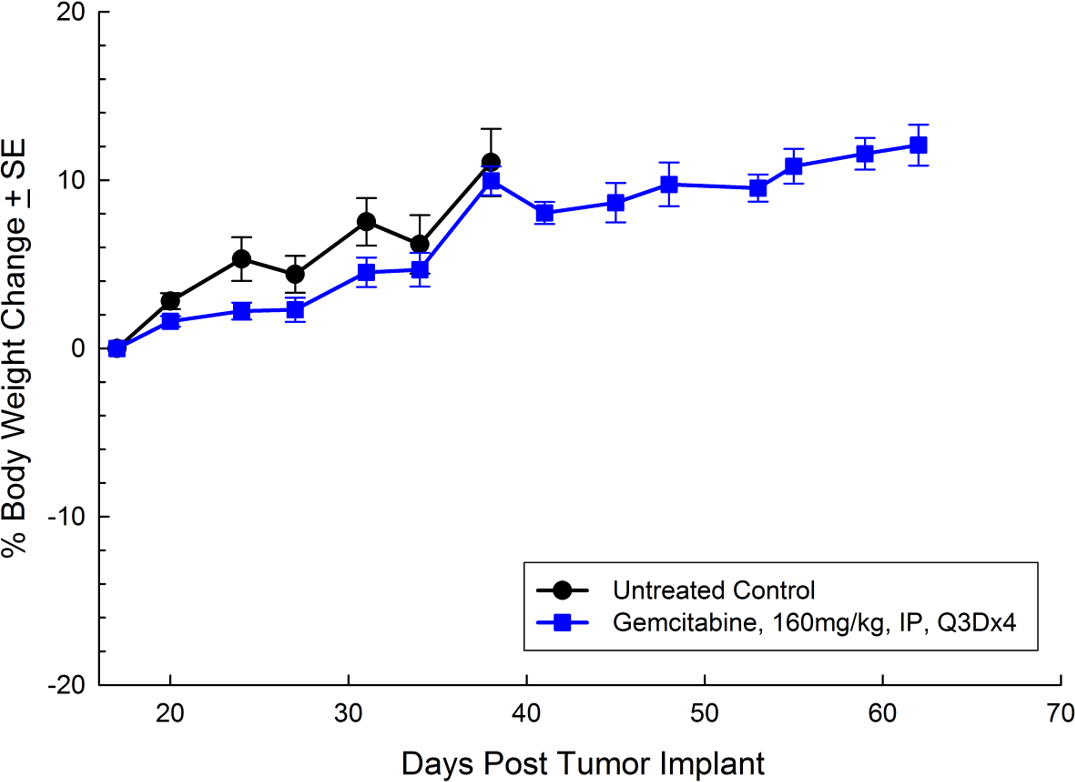
Fig. 1: promedio de carga tumoral de PANC-1 subcutáneo con error estándar
Fig. 2: porcentaje de cambio en el peso corporal de PANC-1 subcutáneo con error estándar
Capan-2
El Capan-2, que se aisló de un hombre caucásico de 56 años de edad con adenocarcinoma ductal pancreático, tiene un crecimiento tumoral subcutáneo que es un poco más lento que el PANC-1, y el volumen del tumor se duplica en unos 12 días y alcanza el tamaño de evaluación (750 mm3) en unos 36 días después del implante. El tratamiento con gemcitabina (112 mg/kg) se tolera bien y produce un retraso del crecimiento tumoral estadísticamente significativo, con una gran cantidad de sobrevivientes sin tumor (ver imágenes 3 y 4).
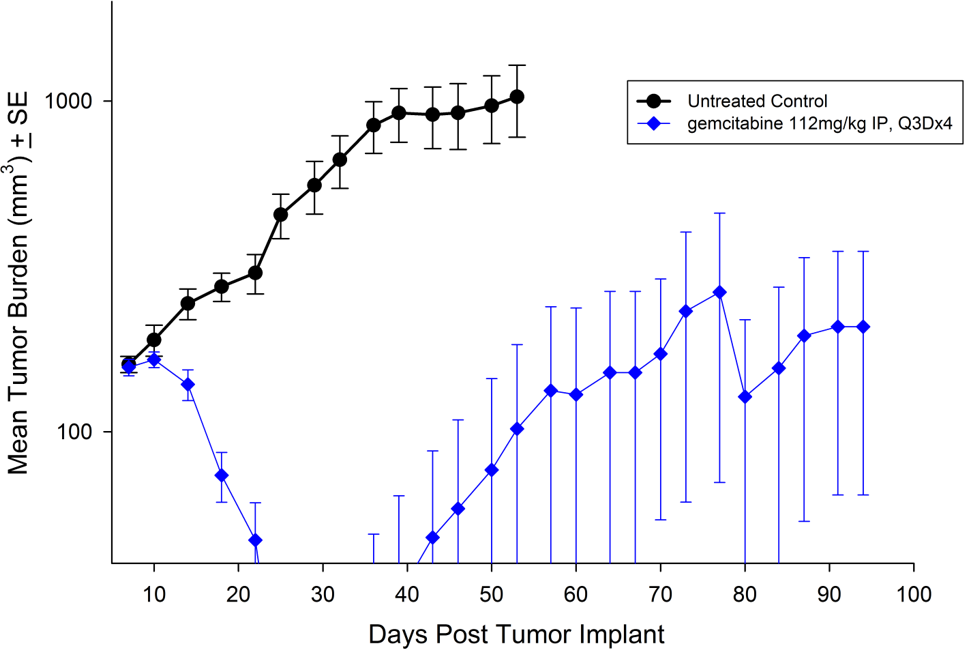
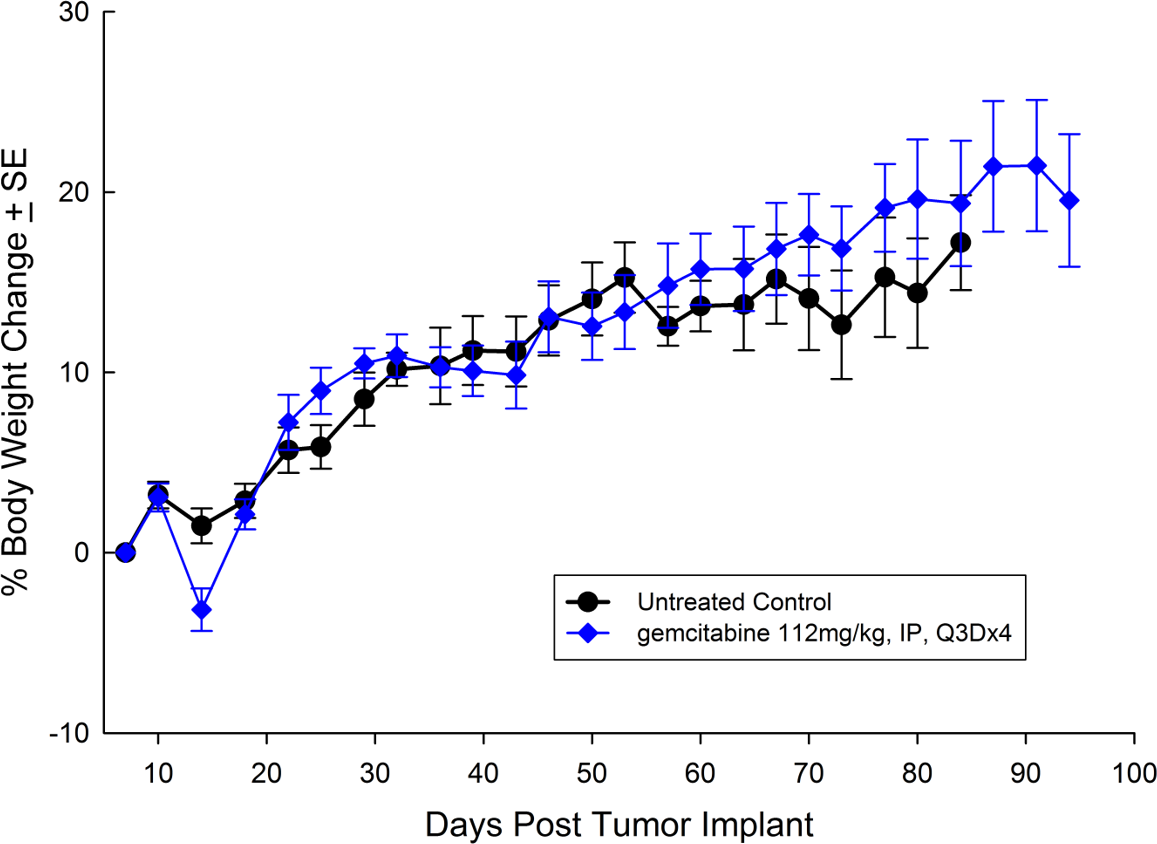
Fig. 3: promedio de carga tumoral de Capan-2 subcutáneo con error estándar
Fig. 4: porcentaje de cambio en el peso corporal de Capan-2 subcutáneo con error estándar
Bx-PC-3
El Bx-PC-3 se aisló de una mujer caucásica de 61 años de edad con adenocarcinoma ductal pancreático. En cuanto a crecimiento tumoral subcutáneo, el volumen del tumor se duplica en unos 16 días y alcanza el tamaño de evaluación (750 mm3) en unos 38 días después del implante. El tratamiento con gemcitabina (80 mg/kg) se tolera bien pero no produce un retraso del crecimiento tumoral estadísticamente significativo (ver imágenes 5 y 6).
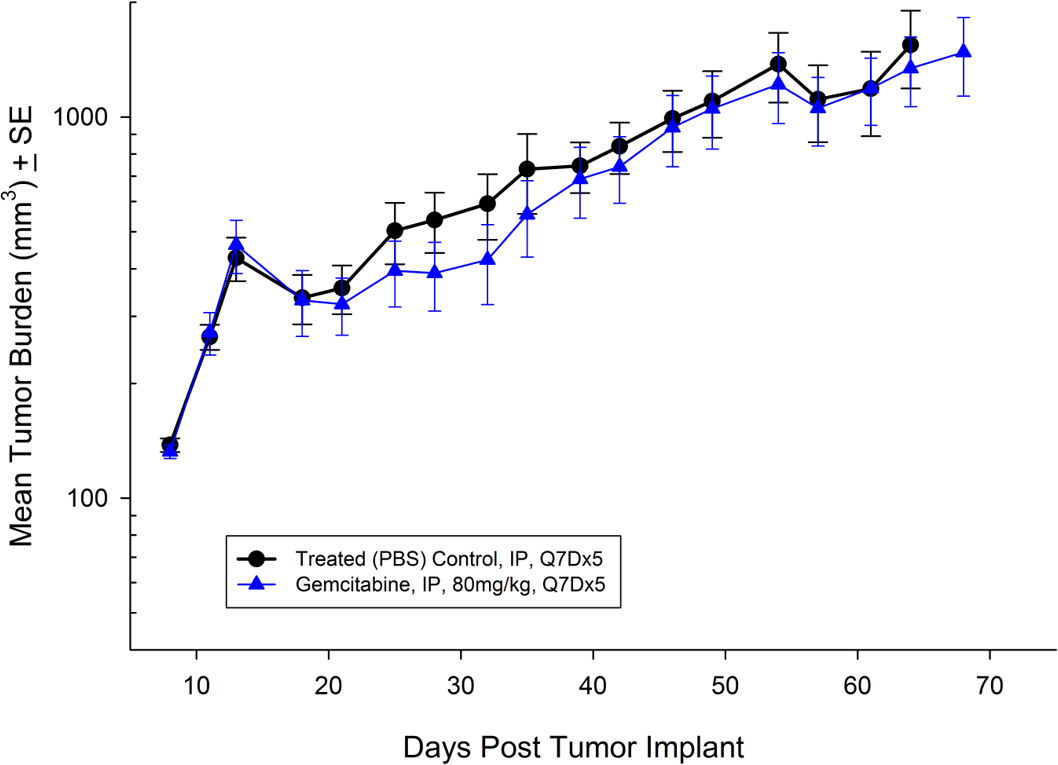
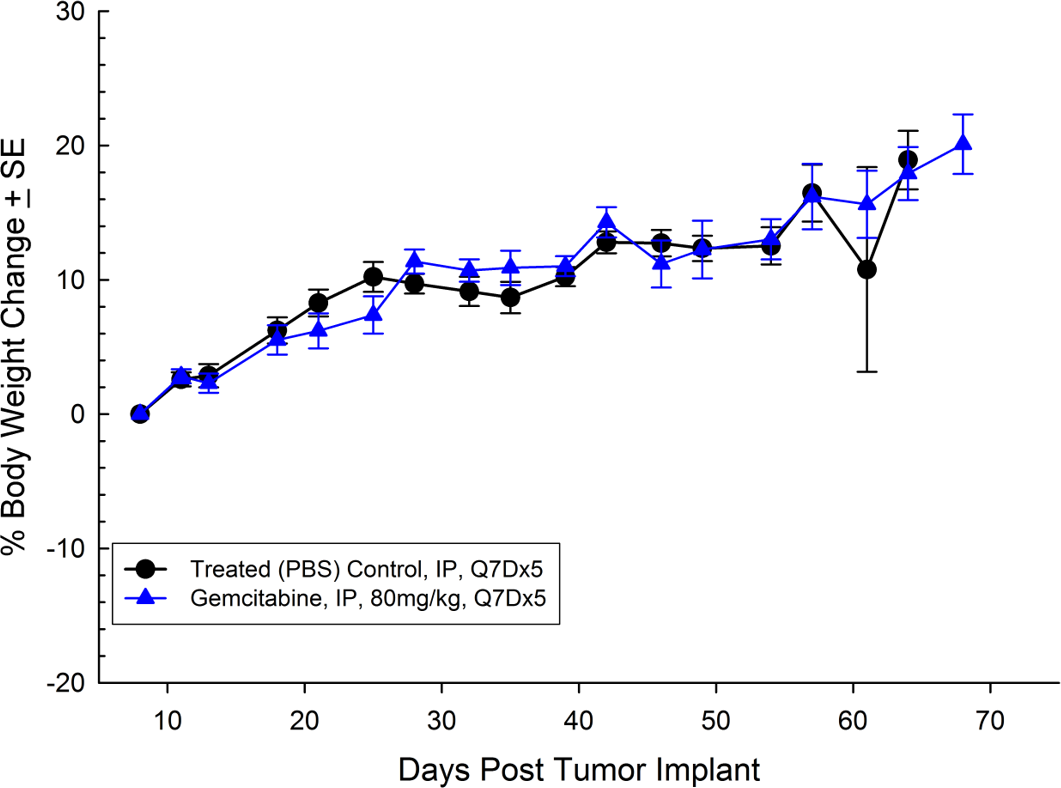
Fig. 5: promedio de carga tumoral de Bx-PC-3 subcutáneo con error estándar
Fig. 6: porcentaje de cambio en el peso corporal de Bx-PC-3 subcutáneo con error estándar
MIAPaCa-2
El MIAPaCa-2 se aisló de un hombre caucásico de 65 años de edad con adenocarcinoma ductal pancreático. Este modelo exhibe un crecimiento tumoral subcutáneo muy agresivo donde el volumen del tumor se duplica en unos 3 días y alcanza el tamaño de evaluación (750 mm3) en unos 21 días después del implante. El tratamiento con gemcitabina (160 mg/kg) se tolera bien y produce un retraso del crecimiento tumoral estadísticamente significativo, donde se observó un sobreviviente sin tumor en el estudio (ver imágenes 7 y 8).
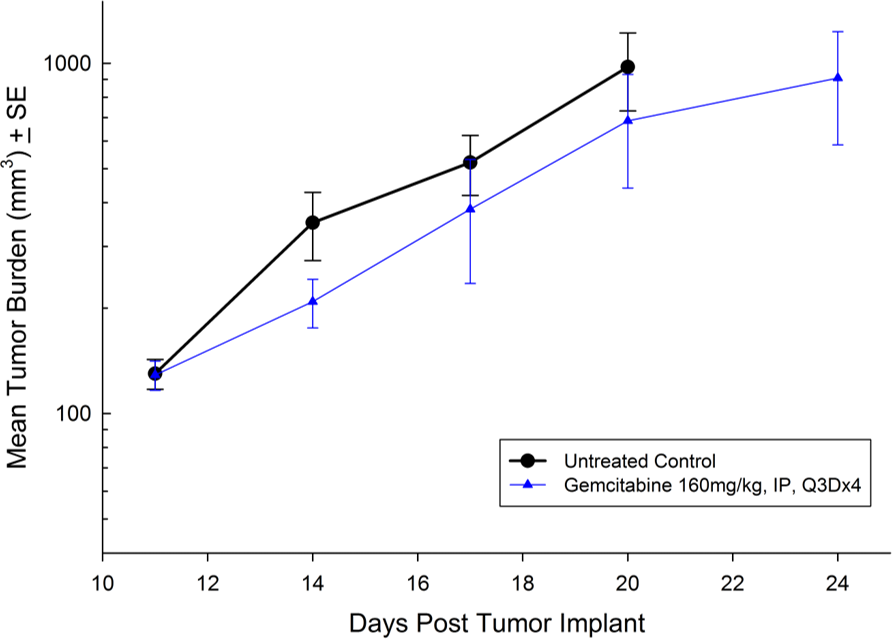
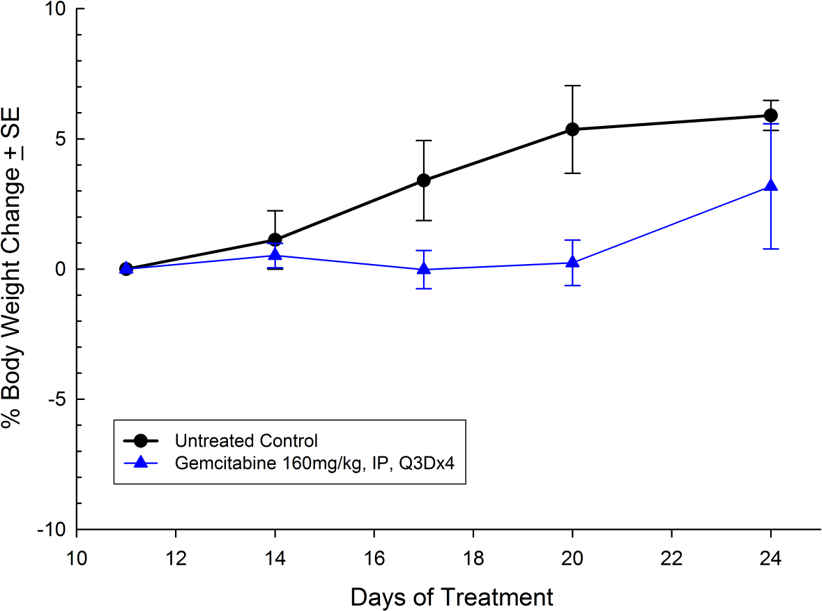
Fig. 7: promedio de carga tumoral de MIAPaCa-2 subcutáneo con error estándar
Fig. 8: porcentaje de cambio en el peso corporal de MIAPaCa-2 subcutáneo con error estándar
Como la respuesta clínica al estándar de atención, la respuesta al tratamiento preclínicamente depende muchísimo de la línea tumoral que se está usando. Existen muchos factores que pueden contribuir a la respuesta o a la falta de la misma en un tratamiento con gemcitabina. Sin embargo, al evaluar varias líneas tumorales diferentes dentro de la misma indicación podemos acceder a información clave sobre la eficacia que podría tener una terapia nueva en la clínica.
Please contact us if you are interested in discussing any of our pancreatic models.
Referencias
Conéctese
Conversemos
Contáctenos