Date: May 2020
Introducción
La línea celular BT-474 tiene una larga historia, pero muchos de nosotros suponíamos que había cumplido su ciclo y se había vuelto obsoleta.
Según American Type Culture Collection (ATCC), la línea celular BT-474 fue creada originalmente en 1978 por E. Y. Lasfargues, quien obtuvo una biopsia tumoral de una mujer de 60 años con carcinoma ductal invasivo de mama en estadio avanzado. Luego la línea celular se clasificó positiva para receptores de estrógenos (ER+), positiva para receptores de progesterona (PR+) y positiva para receptor 2 de factor de crecimiento epidérmico (HER2) (1). Esta información resultó crítica para vincular el uso del modelo BT-474 en investigación preclínica de cáncer de mama a pacientes reales con el mismo perfil genético.
Según la American Association of Cancer Research, aproximadamente un 80% de todos los pacientes con cáncer de mama son ER positivos y ~65% son PR positivos. Los pacientes con cáncer de mama que son tanto ER como PR positivos tiene mayor probabilidad de responder bien a la terapia hormonal. Más aún, ~20% de los casos de cáncer de mama muestran un aumento en la expresión de HER2, vinculada a tumores agresivos y de crecimiento rápido. La relación entre el modelo preclínico BT-474 y los biomarcadores de pacientes, sumada a la extrema necesidad de avances continuos en el tratamiento de cáncer de mama, convirtieron a este modelo en uno altamente deseable para investigaciones tanto in vitro como in vivo.
El reto del BT-474
Todo esto parecía demasiado bueno para ser real. El problema con el BT-474 (y con varios otros modelos de cáncer de mama) es que presenta problemas notorios para el trabajo in vivo.
Cuando se implanta de manera subcutánea o en la grasa mamaria de ratones hembra nude, la tasa de crecimiento tumoral es extremadamente lenta (el tumor tarda más de 20 días en duplicarse), con una variabilidad significativa en el crecimiento tumoral y las regresiones tumorales espontáneas. Estos resultados son consistentes en varios estudios, a pesar de los intentos de ajustar diversas variables como la cepa de ratones (SCID o nude), el material del implante (fragmentos o células tumorales), los suplementos de implante celular (Matrigel® o capa de células alimentadoras) y el suplemento hormonal (estradiol).
Estos problemas convierten al modelo BT-474 en uno difícil para trabajar, y los científicos e investigadores por lo general deben buscar otros modelos con perfiles genéticos similares que faciliten el trabajo y permitan producir datos más confiables.
Sin embargo, como hay muy pocos modelos que reúnen todos los criterios del BT-474 (carcinoma humano de mama que sea ER+, PR+ y HER2+), decidimos seguir trabajando para optimizar el modelo. Además, el avance y acceso a ratones NSG nos permite evaluar el crecimiento del BT-474 en la cepa más inmunodeficiente.
Análisis
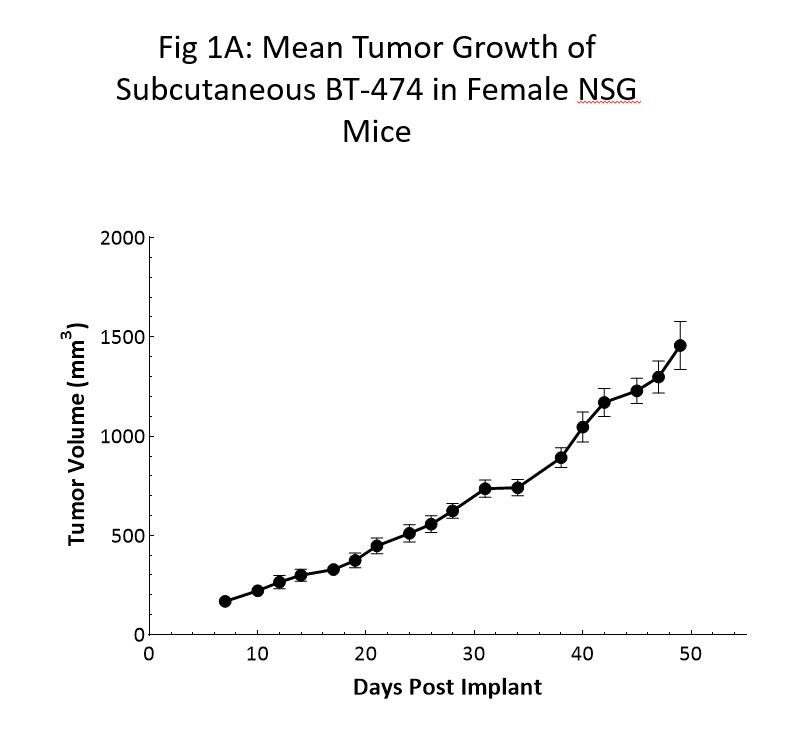
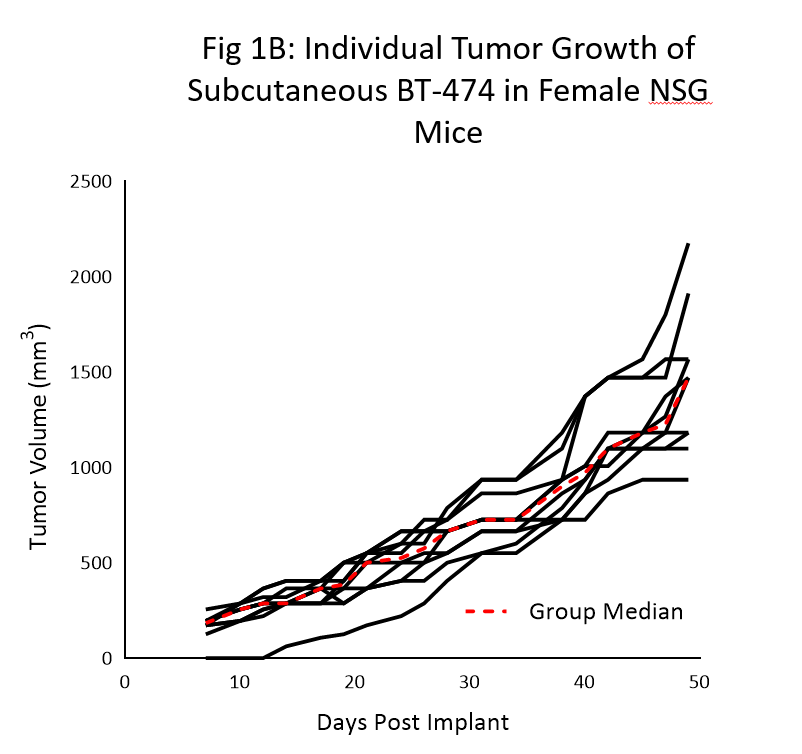
La cinética de crecimiento tumoral del modelo BT-474 en ratones NSG se muestra en la figura 1. El tiempo de duplicación promedio es de ~12 días, con un aumento constante en el incremento del volumen tumoral sin pérdida de peso corporal aparente en relación con el tumor (estos datos no se muestran). El tiempo de 150mm3 (tumores establecidos) fue de 7 días posimplante, y el tiempo de 1000mm3 (tamaño de evaluación) fue de 40 días posimplante.
En los últimos 6 meses re reprodujeron datos similares de cinética de crecimiento en unos cuantos estudios.
Como se puede ver claramente a través de los datos, la utilizacion del ratón NSG fue crucial para el hallazgo de crecimiento confiable y reproducible en este modelo.
Respuesta al tratamiento orientado de HER2
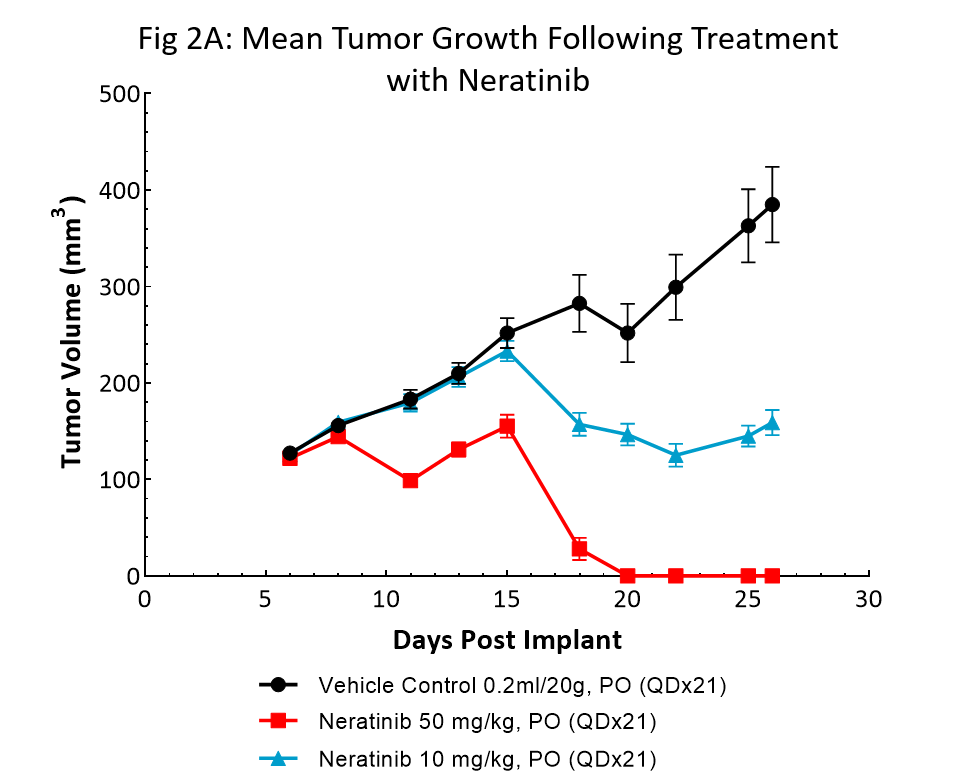
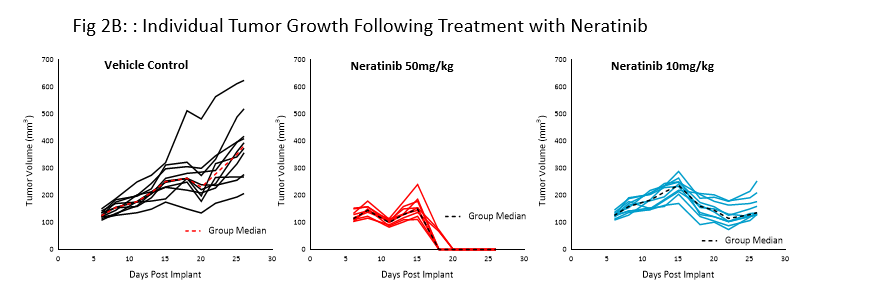
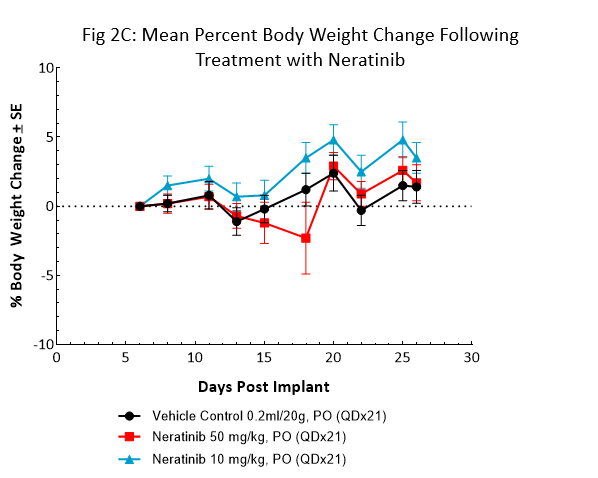
El neratinib (Nerlynx®) es un inhibidor irreversible de la tirosina quinasa Her2 (receptor de crecimiento epidérmico humano 2) y del EGFR (receptor de factor de crecimiento epidérmico) aprobado por la FDA y disponible para administración oral. Se evaluó la respuesta al neratinib tanto a 10 como a 50 mg/kg en ratones NSG con tumores subcutáneos BT-474 tratados a diario durante 21 días consecutivos (fig. 2).
El tratamiento con neratinib resultó bien tolerado en ambas dodis, lo que produjo un cambio mínimo en el peso corporal. El régimen con dosis de 50mg/kg resultó en una regresión total del tumor en todos los ratones. El tratamiento con niveles más bajos de dosis resultó en ~50% de inhibición del tumor, lo que sugiere la respuesta a la dosis. Estos datos aportan evidencia clara de que el modelo BT-474 ha mantenido su sobreexpresión y dependencia de HER2.
BT-474: nueva vida para una potente herramienta preclínica
Dada la necesidad constante de nuevos tratamientos de cáncer de mama orientados, desde terapias de moléculas pequeñas y anticuerpos hasta las celulares, es nuestra responsabilidad optimizar las líneas celulares únicas que tenemos disponibles para investigaciones de descubrimiento farmacológico.
El uso de modelos como el BT-474 que puedan cerrar la brecha entre el modelo preclínico y el paciente con cáncer es crucial. La optimización de nuestro modelo de cáncer de mama BT-474 en ratones NSG supuso un avance sustancial de nuestros modelos de tumores de mama validados, y seguimos evaluando terapias orientadas de HER2, como la herceptina, en el modelo BT-474.
Please contact us to speak with our scientists about how BT-474 or one of our other models can be used for your next oncology study.
Referencias
Conéctese
Conversemos
Contáctenos