Author: Sheri Barnes, PhD, Director, Scientific Development
Date: October 2017
Los investigadores están usando modelos de ratones preclínicos en un esfuerzo por emplear métodos de tratamiento convencionales para linfoma —como radioterapia y quimioterapia— en combinación con agentes inmunomoduladores para tratar con mayor eficacia esta enfermedad. We have developed the syngeneic A20 tumor model, a B cell lymphoma, to support these immuno-oncology applications.
Los linfomas representan un grupo altamente heterogéneo de cáncer de células linfoides. Se pueden originar en las células B o T, pero los linfomas derivados de células B, específicamente el linfoma no Hodgkin (LNH), son los más prevalentes. Los linfomas se puede diagnosticar en niños y adolescentes, pero la incidencia de linfoma aumenta significativamente con la edad y la edad promedio de diagnóstico es a los 67 años. Se estima que en el 2017 se diagnosticarán 72.240 nuevos casos de LNH en los Estados Unidos y 20.140 pacientes fallecerán a causa de esta enfermedad. La tasa de supervivencia de cinco años para LNH es relativamente alta en un 71% y la recurrencia suele darse dentro de los cinco años de tratamiento1, por lo que el desarrollo de nuevas estrategias de tratamiento para el linfoma es fundamental para la supervivencia a largo plazo de estos pacientes.
Habiendo visto el impacto de la inmunoterapia en otros tipos de cáncer, los investigadores están usando modelos de ratones preclínicos en un esfuerzo por emplear métodos de tratamiento convencionales para linfoma —como radioterapia y quimioterapia— en combinación con agentes inmunomoduladores para tratar con mayor eficacia esta enfermedad. We have developed the syngeneic A20 tumor model, a B cell lymphoma, to support these immuno-oncology applications. El modelo A20 proviene de un sarcoma de células reticulares espontáneo de un ratón Balb/c anciano.2 Se ha reportado que los tumores A20 expresan altos niveles de PD-L13 y responden a anticuerpos inmunomoduladores. Tomando estos datos en conjunto, el A20 resulta un modelo atractivo para usar en desarrollo farmacológico para inmunoterapias.
El tiempo de duplicación del A20 es de ~4-5 días, una velocidad de crecimiento moderada en relación con otros modelos singeneicos, lo que podría facilitar una duración de dosificación más prolongada para que los agentes de prueba generen su actividad antitumoral. La imagen 1 demuestra el crecimiento promedio (1A) e individual (B-E) de tumores de control comparados con los tratados con un anticuerpo inmunomodulador. Con la dosificación iniciada en el día 3 tras el implante para inhibidores de puntos de control anti-PD-1 y anti-PD-L1, y en el día 10 tras el implante para el anti-GITR agonista, la respuesta antitumoral es sorprendente. Esperamos que iniciar la dosificación con estos agentes una vez que los tumores A20 son palpables dará lugar a mejoras en combinación con moléculas candidato.
Figura 1: crecimiento promedio e individual de tumores A20 tras inmunoterapia
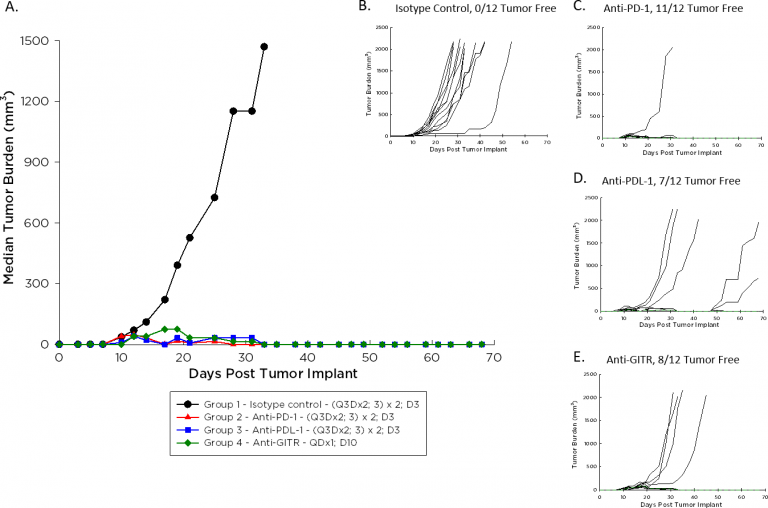
Para investigar los efectos antimoduladores de anti-GITR en el tumor A20 analizamos las poblaciones de células T y mieloides en el tumor una semana después del tratamiento. Los resultados se ilustran en la imagen 2. Con el tratamiento con anti-GITR, la proporción de células CD8+/Treg aumenta drásticamente (imagen 2A). Este aumento indica la participación del sistema inmunológico huésped, lo que también se refleja en la reducción de la carga tumoral (imagen 1). Por otro lado, los cambios en poblaciones de células mieloides fueron modestos. Mientras que algunas poblaciones de células mieloides no presentaron ningún cambio con el tratamiento, se observa una tendencia hacia una disminución en el porcentaje de CSDM-M acompañado por un aumento en el porcentaje de macrófagos M1 con el tratamiento con anti-GITR comparado con el control de isotipo (imagen 2B).
Figura 2: perfil inmune de tumores A20 tras tratamiento con anti-GITR
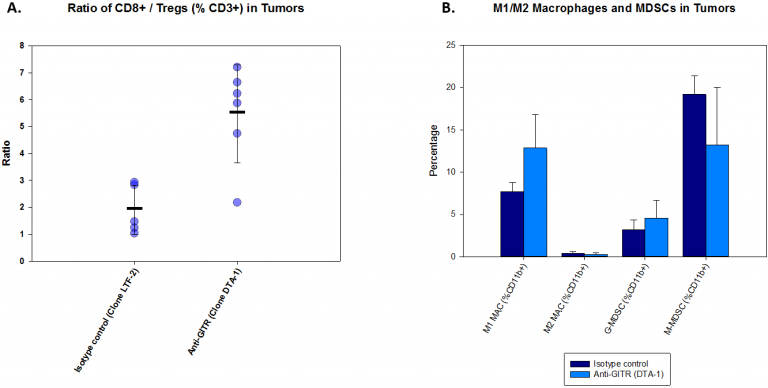
Además de la promesa de la inmunoterapia, durante el tratamiento clínico de linfomas se suele usar radioterapia y normalmente se administra en combinación con otros agentes. We employ the Small Animal Radiation Research Platform (SARRP) by XStrahl for modeling focal beam radiation (see our related blog and poster), and investigated a single dose range of 5-20 Gy against A20 tumors. El crecimiento tumoral promedio (figura 3A) e individual (figura 3B-E) tras el tratamiento se ilustra abajo. Los tumores A20 responden a la radiación en todas las dosis, y dos ratones cada uno a los niveles de dosis de 10 y 20 Gy tuvieron respuestas completas duraderas casi 70 días después del implante. Estos animales permanecieron libres de tumores a pesar de una reprueba con una segunda inyección de células A20, mientras que los tumores crecieron según lo esperado en animales sin tratar de la misma edad (datos no mostrados).
Figura 3: curvas de crecimiento promedio e individual de tumores A20 tras radiación focalizada
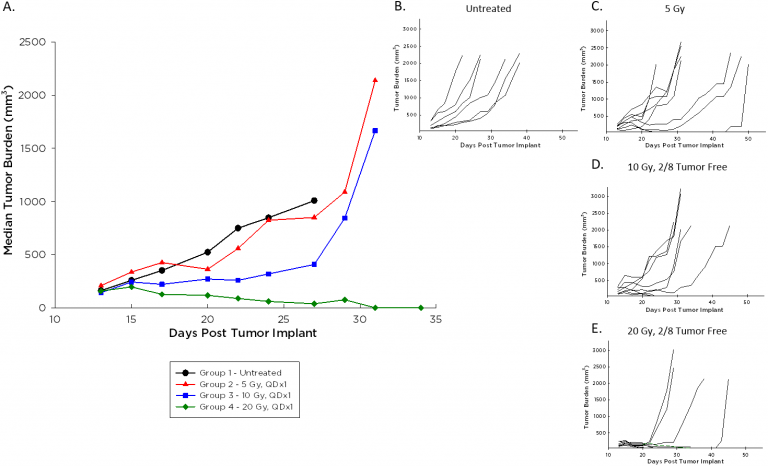
El modelo A20 constituye un sólido medio preclínico para el estudio de linfoma de células B. La respuesta del modelo A20 a inhibidores de puntos de control, inmunoantagonistas coestimuladores y radioterapia lo convierten en un modelo atractivo para usar en el entorno de la inmuno-oncología preclínica.
Referencias
1Howlader N, Noone AM, Krapcho M, Miller D, Bishop K, Kosary CL, Yu M, Ruhl J, Tatalovich Z, Mariotto A, Lewis DR, Chen HS, Feuer EJ, Cronin KA (eds). SEER Cancer Statistics Review, 1975-2014, National Cancer Institute. Bethesda, MD, https://seer.cancer.gov/csr/1975_2014/, según la presentación de datos de SEER de noviembre de 2016, publicado en el sitio web de SEER en abril de 2017.
2Kim KJ, Kanellopoulos Langevin C, Merwin RM, Sachs DH, Asofsky R (1979) Establishment and characterization of BALB/c lymphoma lines with B cell properties. Journal ofImmunology, 122(2): 549–554.
Conéctese
Conversemos
Contáctenos