Author: Dylan Daniel, PhD, Director, Scientific Development
Date: December 2016
El cáncer de mama es la segunda malignidad más mortal después del cáncer de pulmón en mujeres en los Estados Unidos, y para el 2016 se espera una incidencia de 246.000 nuevos casos y 40.450 muertes. Existen muchas opciones de tratamiento para el cáncer de mama, entre ellas cirugía, radioterapia, terapia con antiestrógenos, terapias focalizadas (por ej. trastuzumab) y quimioterapia. A pesar de estos avances terapéuticos, la metástasis sigue siendo una causa significativa de mortalidad. En los últimos cinco años se han hecho grandes avances en inmunoterapia con la aprobación de cuatro inhibidores de puntos de control inmunitario de células T. Aunque ninguno de estos inhibidores de puntos de control están aprobados para el cáncer de mama, en este momento se están haciendo más de 60 ensayos clínicos en cáncer de mama con inhibidores de puntos de control contra PD-1 o PD-L1 y hay más de 20 ensayos clínicos en curso con inhibidores de CTLA-4.
Como los inhibidores de puntos de control y otras clases de inmunoterapias requieren un sistema inmunológico intacto para generar actividad, los modelos en ratones singeneicos de cáncer mamario son una opción importante para la realización de pruebas preclínicas de nuevos agentes. Labcorp has fully characterized the 4T1-luc2 mammary carcinoma model derived from Balb/c mice as an orthotopic model to support studies with novel immuno-oncology agents. Los tumores 4T1-luc2 ortotópico hacen metástasis en los ganglios linfáticos y los pulmones, por lo que resulta un modelo valioso para estudiar el efecto de terapias tanto en el tumor principal como de la metástasis usando imagenología por bioluminiscencia. El crecimiento de tumores 4T1-luc2 es equivalente en cepas inmunodeficientes y ratones Balb/c inmunocompetentes lo que sugiera que el 4T1-luc2 es un tumor débilmente inmunogénico (Imagen 1).
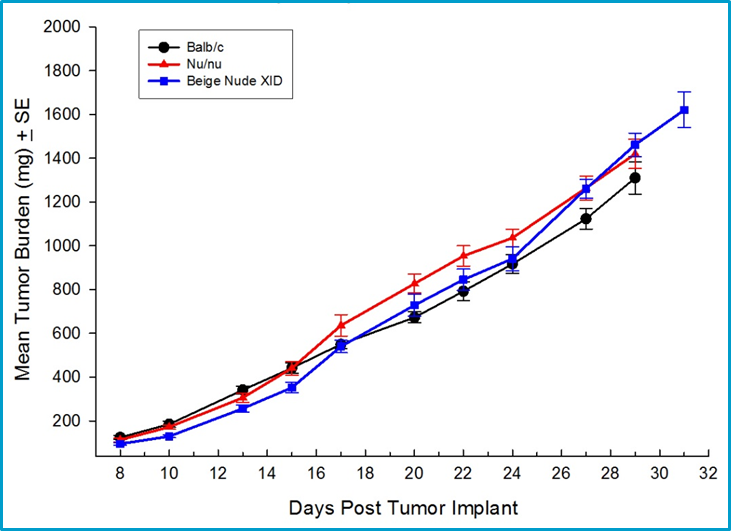
Imagen 1: Crecimiento ortotópico de 4T1-luc2 en varias cepas de ratones incluso ratones Balb/c singeneicos.
Los estudios de eficacia con anticuerpos a PD-1 o PD-L1 se ven perjudicados por una reacción de hipersensibilidad fatal en ratones con tumores 4T1.1 Es posible administrar dos dosis sin toxicidad, pero no es posible seguir administrando más dosis. Por tanto se evaluó la eficacia de un anti-CTLA-4 en combinación con radiación localizada. Se usó un anticuerpo anti-CTLA-4 de hámster, e inesperadamente el control de isotipo de hámster exhibió actividad significativa en algunos ratones, (imagen 2A), que fue idéntica a la actividad del anti-CTLA-4 (imagen 2B). Hubo un beneficio terapéutico asociado a la radiación localizada (imagen 2C), pero no se vio una mejora clara con la combinación de radiación y anti-CTLA-4 (imagen 2D).
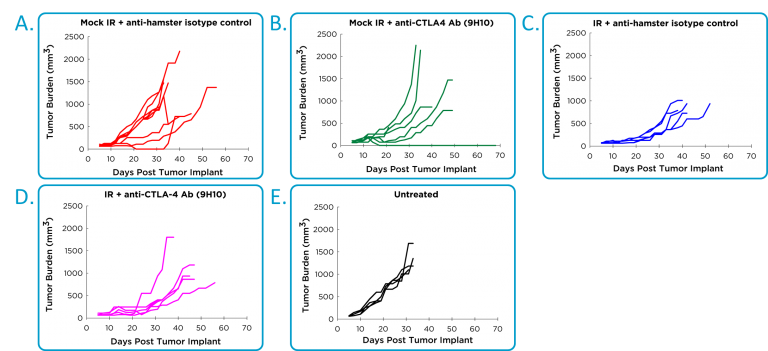
Imagen 2: Eficacia de anti-CTLA-4 y radioterapia localizada en modelo de tumor mamaria 4T1-luc2 ortotópico.
La carga metastásica se evaluó usando imagenología por bioluminiscencia, y aquí mostramos imágenes representativas de la progresión metastásica en ratones sin tratar (imagen 3A). Los ratones tratados con anti-CTLA-4 tuvieron una carga tumoral metastásica reducida en comparación con los ratones bajo tratamiento de control de isotipo (imagen 3B). La radiación localizada también produjo una reducción significativa en la carga metastásica; sin embargo, no parece haber ninguna mejora más allá de la actividad con un solo agente de anti-CTLA-4 en el grupo de tratamiento combinado.
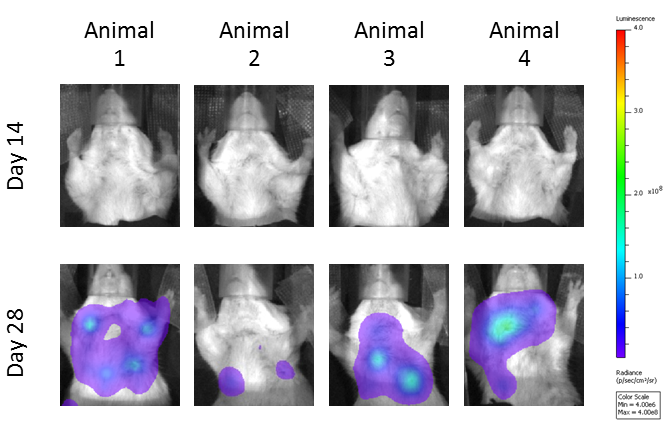
Imagen 3: Evaluación de carga tumoral metastásica con el tiempo mediante imagenología por bioluminiscencia:
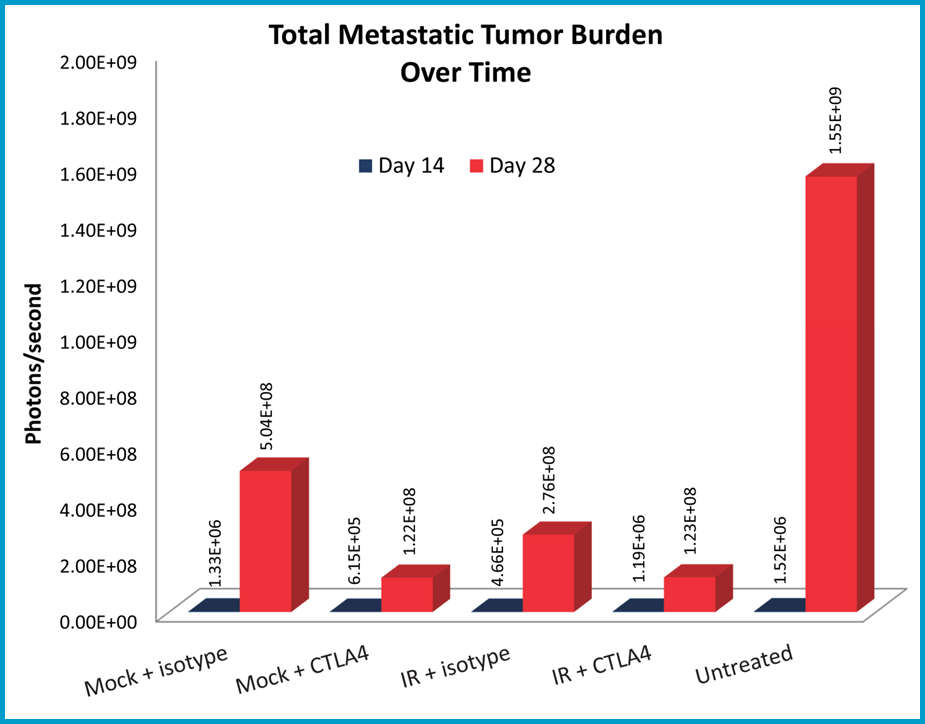
Imagen 3B: Cuantificación de carga metastásica y respuesta al tratamiento.
La radiación en este estudio se localizó usando protectores de plomo para reducir la radiación en todo el cuerpo; sin embargo, algunos animales igual exhibieron indicios de toxicidad por radiación. Labcorp now offers focal beam radiation capabilities using the small animal radiation research platform (SARRP) by Xstrahl which reduces systemic radiation toxicity.
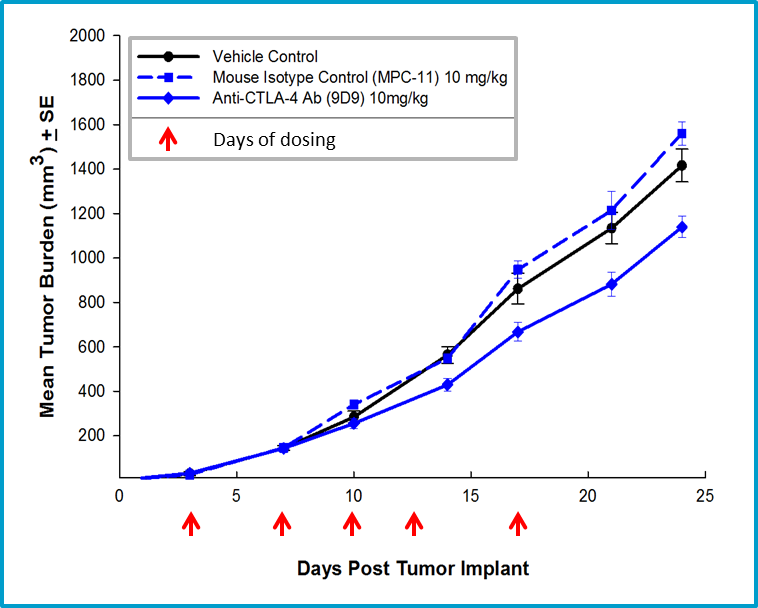
Imagen 4: Eficacia de terapia con anti-CTLA-4 con anticuerpo anti-CTLA-4 de isotipo de ratón.
La actividad antitumoral no específica asociada al uso de un anticuerpo de hámster en el modelo 4T1-luc2 dio lugar un estudio subsiguiente usando un anticuerpo anti-CTLA-4 de ratón. El tratamiento con anti-CTLA-4 de ratón tuvo una actividad mínima en el modelo 4T1-luc2 (imagen 4), pero se puede usar para combinaciones en estudios patrocinados por el cliente con nuevos agentes inmuno-oncológicos. Además contamos con una variedad de análisis inmunes de citometría de flujo de tumores 4T1-luc2, incluyendo cuantificación de células T CD4 T, células T CD8, células T reguladoras, CSDM granulocíticas, CSDM monocíticas y macrófagos asociados a tumores (MAT) M1 y M2 (imagen 5). El modelo está ampliamente caracterizado y disponible para estudios patrocinados por el cliente con agentes o inmunoterapias nuevas que pueden combinarse bien con inmunoterapias disponibles comercialmente. Please contact us for further information and find out how Labcorp can help with your next study.
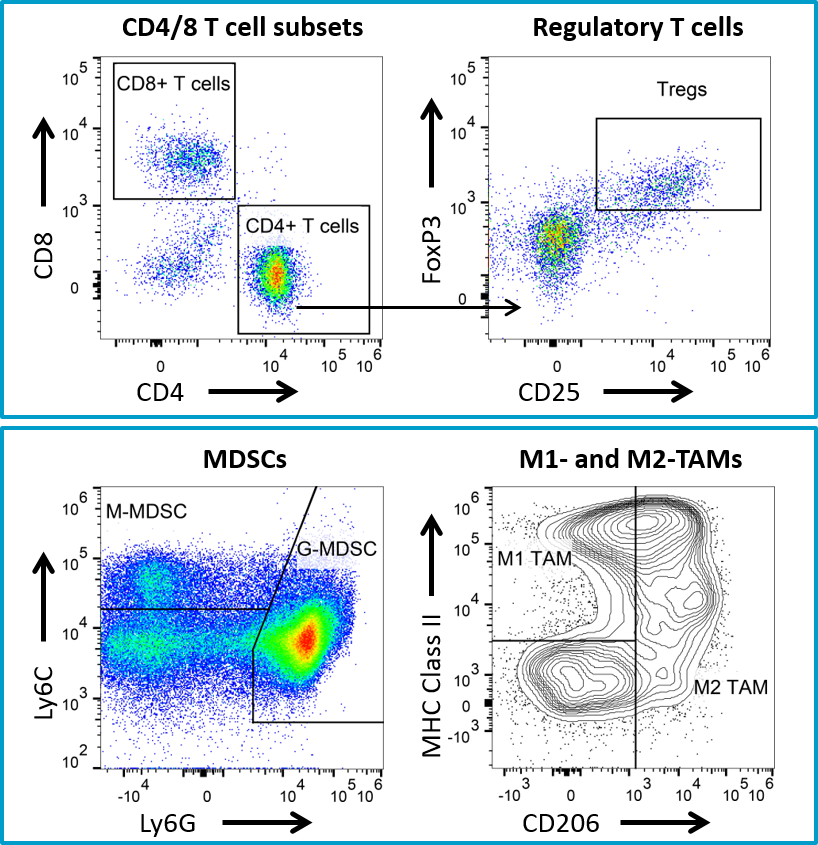
Imagen 5: Análisis inmune por citometría de flujo para tumores 4T1-luc2.
1Mall et al., OncoImmunology (2016), Vol. 5 (2): e1075114
Nota: Los estudios se realizaron de conformidad con la normativa de bienestar animal vigente en un establecimiento con acreditación de AAALAC
Referencias
Conéctese
Conversemos
Contáctenos